LEQEMBI 皮下注射劑型的最新研究進展
衛材株式會社宣布,將在第16屆阿爾茨海默病臨床試驗(CTAD)年會上公布其阿爾茨海默病(AD)治療藥物LEQEMBI®(lecanemab-irmb)100 mg/mL的III期Clarity AD研究的最新數據以及正在開發的皮下制劑的新數據,該會議將于2023年10月24日至27日在美國馬薩諸塞州波士頓舉行。會議上,除了介紹衛材LEQEMBI的數據外,還將介紹E2511(一種研究性原肌球蛋白受體激酶A(TrkA)陽性變構調節劑(PAM))的I期數據以及公司AD產品線的其它研究。在此次會議上,衛材將通過五場口頭報告和十場海報展示來介紹數據和研究成果。BioArctic 將就 lecanemab 作口頭報告。
最新專題研討會4——Lecanemab治療早期阿爾茨海默病:長期療效、預測性生物標志物和新型皮下給藥
在美國東部時間10月25日17:25-18:05舉行的一次突破性研討會上,衛材將展示Clarity AD可選tau PET縱向子研究的最新數據。該演示將包括對低和中等+高tau亞組的事后分析,低tau亞組代表疾病的早期階段,特別是在III期核心研究和開放標簽擴展研究中進行研究。此外,還將介紹研究皮下制劑的最新情況,包括中期安全性和淀粉樣蛋白 PET 對大腦中淀粉樣蛋白的影響。
Christopher van Dyck醫學博士、Keith Johnson醫學博士和Reisa Sperling醫學博士將在衛材Michael Irizarry醫學博士(公共衛生碩士)主持的小組討論中討論這些發現。
本次研討會的網絡直播可在衛材株式會社網站上觀看。
衛材神經內科臨床研究高級副總裁、臨床證據生成部副首席臨床官Michael Irizarry醫學博士表示,"阿爾茨海默病是一種漸進性的頑固疾病,需要早期診斷和持續治療。LEQEMBI能夠清除高毒性原纖維,從而支持阿爾茨海默病的神經元功能,而高毒性原纖維在斑塊被清除后仍會繼續導致神經元損傷和死亡。我們期待在2023年CTAD上分享新的LEQEMBI低tau亞組數據和皮下注射數據。"
其它主要口頭報告包括
Lecanemab:lecanemab和donanemab與不同淀粉樣蛋白-β的結合概況(OC19,由BioArctic公司介紹)。
新型TrkA調節劑E2511在 I期臨床研究中與中樞神經系統膽堿能靶點結合(OC34)。
新型CSF tau生物標志物可用于散發性阿爾茨海默病的疾病分期(OC2)。
衛材演講列表如下:
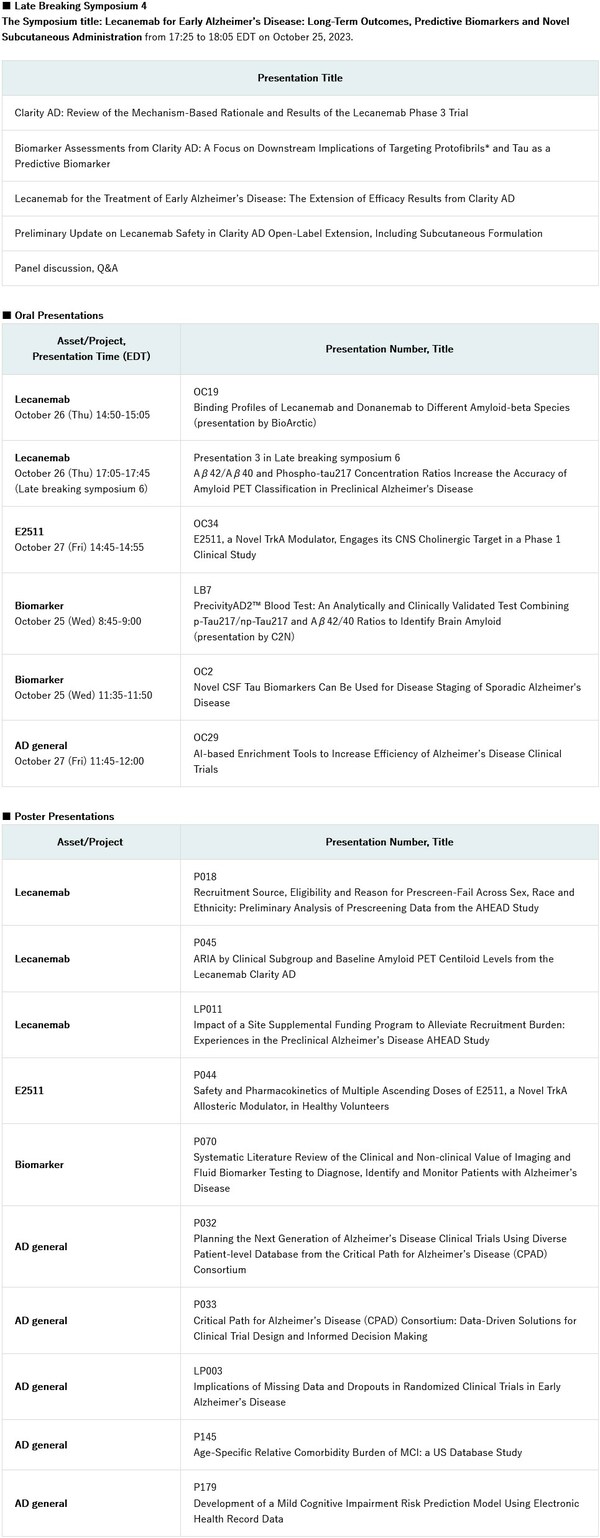
本新聞稿討論了藥物在開發中研究性用途,并非傳達關于療效和安全性的結論,不保證任何研究性藥物將成功完成臨床開發或獲得藥品監管機構批準。
(新媒體責編:wa123)
聲明:
1、凡本網注明“人民交通雜志”/人民交通網,所有自采新聞(含圖片),如需授權轉載應在授權范圍內使用,并注明來源。
2、部分內容轉自其他媒體,轉載目的在于傳遞更多信息,并不代表本網贊同其觀點和對其真實性負責。
3、如因作品內容、版權和其他問題需要同本網聯系的,請在30日內進行。電話:010-67683008
人民交通24小時值班手機:17801261553 商務合作:010-67683008轉602 E-mail:zzs@rmjtzz.com
Copyright 人民交通雜志 All Rights Reserved 版權所有 復制必究 百度統計 地址:北京市豐臺區南三環東路6號A座四層
增值電信業務經營許可證號:京B2-20201704 本刊法律顧問:北京京師(蘭州)律師事務所 李大偉
 京公網安備 11010602130064號 京ICP備18014261號-2 廣播電視節目制作經營許可證:(京)字第16597號
京公網安備 11010602130064號 京ICP備18014261號-2 廣播電視節目制作經營許可證:(京)字第16597號



